2018年11月6日更新

こんにちは、心リハ太郎です。
左室駆出率(LVEF)は心臓の収縮能力を示す重要な指標の1つで、左室駆出分画とも呼ばれます。
LVは左心室(left ventricle)という意味です。
一般的にはLVを略してEFと呼ばれることも多いですね。
心臓病や心臓リハビリに詳しくない人でも、
EFが低い = 心臓が悪い
と考える程度に有名な指標、それがEFです。
しかし、何故EFが悪いのがよくないのか、と聞かれてしっかりと答えられる人は意外に少ないのではないでしょうか?
また、EFが悪くないのに心臓が悪いケースがあるのは何故なのか、という問いに答えられる人の数はもう少し減るかもしれません。
以前は、EFがよければ心臓は問題ないね、という考え方が循環器医でも心リハスタッフでも主流でした(今でもそういう人はいますね)。
これは2000年代くらいまでは
- EFが悪くなる病気が心臓病治療の大きな柱だった
- そのため治療のエビデンス(科学的証拠)もEFが悪くなる心臓病に多かった
- EFが低下する病気が心臓リハビリテーションの主な対象だった
からです。
EF40%以下が慢性心不全の心臓リハビリテーション適応基準の1つになっているのは、心不全のエビデンスのほとんどがEFが低下した人たちを対象に作られていたという理由です。
ですが、最近になって様々な調査で、EFが良くても心臓が悪い人が意外なほど多いことが分かってきました。
そして心臓リハビリテーションもEFのよい心不全患者さんを対象にするケースが増えてきました。
つまり、EFだけで心臓の機能(働きの良し悪し)を判断し、リハビリテーションを行う時代は終わったということです。
ただし、心臓を理解するにあたってEFが重要であることは今も昔も変わりません。
EFは心臓病を対象にした医療に携わる人(場合によっては患者さん本人や家族)にとって必ず理解しておくべき指標で、その有用性と限界を把握しておくことは非常に大事です。
EFを理解するには、
- EFを見れば分かること
- EFを見ると想像できること
- EFを見るだけでは分からないこと
を切り分けられるようになることが重要です。
そこで、この記事では、
- EFとは何か?
- EFが悪くなる理由は?
- EFが悪くないのに心臓が悪い理由は?
- 運動のリスク評価にEFをどう活かす?
ということを解説していきます。
EFとは何か?
EFが悪い人は心臓が悪いと言ってよいか?
と聞かれたら、答えはYESです。
なぜなら心臓の動きが悪くならなければEFは悪くならないからです。
心臓は筋肉を収縮させて全身に血液を送るポンプですから、その筋肉の動きが悪くなるということは心臓が悪くなるということです。
では
EFとは何?
と聞かれてみなさんはどう答えるでしょうか?
そもそもどうしてEFが心臓の評価に使われているのでしょうか?
少し歴史や検査法を紐解きながら、EFについての理解を進めてみましょう。
心臓の評価にEFが使われはじめた経緯
EFは、心臓の血管(冠動脈)が詰まって心臓の筋肉が死んでしまう心筋梗塞という病気を中心とした虚血性心疾患や、心臓の筋肉が変性・変形して正常に動かなくなる拡張型心筋症などの心臓病の評価で主に用いられます。
虚血性心疾患や拡張型心筋症は、心臓の筋肉(心筋)の動きが弱くなり、心臓が出す血液の量が減る病気の代表です。
このような病気で、
- 心臓の動き
- 心臓が出せる血液の量(心拍出量)
を評価できると、どれだけ心臓が悪いのか(重症度)を客観的に理解し、効果的な治療ができるようになります。
この評価に心臓カテーテル技術の発展が関係しています。
心臓カテーテル技術の開発と発展
心筋梗塞では、心臓カテーテル検査や心臓カテーテル治療というものが行われます。

心臓カテーテル検査(北海道心臓病協会HPより)
カテーテルとは細い管のことです。
カテーテルによる心臓の検査や治療は、フォルスマンというドイツ人医師によって行われた自分に対するとんでもない人体実験から始まりました。
医療の挑戦者たち(4)ゴムのチューブを血管から心臓へ。自らの体で挑んだ実験が、心臓カテーテル法を生んだ。(ヴェルナー・フォルスマン)
これ、マジですごいです。
尿道カテーテルを自分の血管(静脈)に入れて押し進め、レントゲン室で自分の心臓にカテーテルが到達しているのを確認するという狂気の沙汰としか思えない行為をしているんですね。
正直言って、考えるだけでおしっこちびるレベルです。
※実際は死体を使ってさまざまな実験を行ったのちに用意周到に実施されたそうです。
その顛末は上記のリンクで確かめていただくとして、このような先人の冒険的な試みの積み重ねの末に、心臓カテーテル検査というものが開発・実用化されたのです。
造影剤を使って心臓と血流を見ることができるようになった
この心臓カテーテル検査の特徴の1つは、カテーテルの中に造影剤を流して心臓に送り込むことができということです。
今は超音波を使ったエコー検査や、MRIによる心臓の撮影など、様々な技術の進歩があり、心臓の動きや血流を体の外から見ることができます。
が、昔は体の中を確認する方法は血液を写すことのできないレントゲン撮影か解剖くらいしかなかったのです。
解剖すると死んでしまいますので、実質選択肢はレントゲン撮影1択となります。
先ほど言ったようにレントゲンには血液が写りませんから、心臓の中の血液の動きは外から見ることができません。
でも心臓の中で血液がどう動いているのかを知りたい!
そこで造影剤の登場です。
造影剤は、X線を当てると色がついて撮影される物質です。
血液に造影剤を混ぜれば色がついて見えます。
そこで心臓カテーテルを使って造影剤を心臓に送り込めばレントゲン撮影で血液が見えるじゃん!
と思いついた人がいたのですね。
そのアイディアが実用化され、心臓カテーテルを使って造影剤を血液中に流すことで、心臓の血管(冠動脈)の血流をみたり、心臓内の血液の動きをみたりすることができるようになったのです。
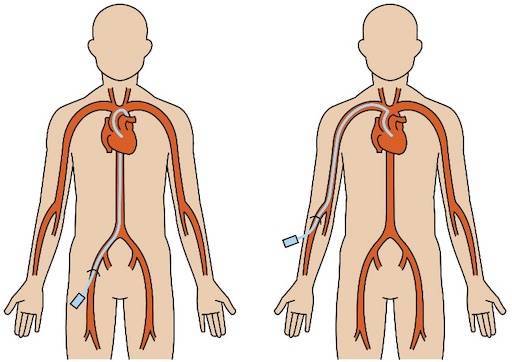
心臓カテーテルの入れ方(北海道心臓協会フリーイラスト集より)
心臓で1番大事な心拍出量は測定が難しい
心臓のポンプ機能を最もよく表すのは、心拍出量(CO: cardiac output)です。
心拍出量は心臓が1分間で送る血液量のことです。
心拍出量は心臓カテーテル検査の1つ、肺動脈カテーテル(商品名のスワンガンツカテーテルという名前で呼ばれることも多い)を使い、心臓からの血流を直接測定して決定するのがゴールデンスタンダード(1番信頼性が高い方法として認められること)になってます。

肺動脈カテーテル(Wikipediaより)
ただ、スワンガンツカテーテルは右心室を通して肺動脈までカテーテルと測定器具を送り込むという非常に侵襲的で簡単に実施できない検査のため、なかなか心拍出量は測定できないのが問題です。
そこでもう少し侵襲度の少ない心臓の機能評価を行う必要がありました。
左室造影検査(LVG)
心臓カテーテル検査のうち、左心室に造影剤を入れて、左心室内の血液や心臓の動きを見る検査を左室造影検査(LVG)といいます。
造影剤を左心室に入れると、左心室の中の血液が黒く写ります。
心臓の壁に囲まれているので、造影剤は心臓の内腔の形に沿って広がります。
心臓が収縮したり、拡張したりすると、造影剤が写す心臓内腔の形も変わります。
すると心臓内腔の形や大きさ、筋肉の動きがわかります。
さらにどこか動きの悪いところがあるかどうかもわかります。
この方法を使うと、心臓のどこの壁がどのくらい動きが悪いのかを示すことができます。
また、血液が心臓から押し出されていくのを撮影して、心臓からどれくらいの血液が出て行くか、弁の逆流はないかなどもわかるのです。
この左室造影検査によって、見ることのできなかった心臓の中の状態を把握することができるようになったのです。
左室造影検査(LVG)による壁運動異常の評価方法
心臓の壁の動きが悪いことを壁運動異常と言います。
左室造影検査での壁運動異常を評価する方法はAHA(アメリカ心臓病学会)分類が用いられます。

http://www.igaku.co.jp/pdf/1201_heart-03.pdf より抜粋引用
2つの撮影角度からみた計7部位の壁運動異常を以下の6区分で評価します。
- 正常収縮(normal)
- 収縮低下(reduced)
- 無収縮(none)
- 収縮期膨隆(dyskinetic)
- 心室瘤(aneurysmal)
- 定義不能(undefined)
1の正常収縮と6の定義不能以外、つまり2〜5はその部位の壁運動異常があるという評価で2→5の順に悪くなります。
収縮期膨隆(しゅうしゅくきぼうりゅう)とは、心臓が収縮するときにその部分だけ逆に膨らむような動きをすることです。奇異性収縮(きいせいしゅうしゅく)とも言います。
収縮期膨隆があると、膨らむ部分に血液が逃げて圧力が上がりにくくなり、心拍出量が落ちます。
心室瘤(しんしつりゅう)とは心臓の壁が薄くなり、瘤のように膨らんできている状態のことです。
心室瘤があるとやはり瘤の部分に血液が逃げますし、その部分は心臓の収縮に全く関与しなくなりますので、心拍出量が低下します。
このように心臓の動きのよさはAHA分類で部位別の壁運動異常の有無と重症度で評価します。
(心臓エコー検査も少し違いますが大体同じです。)
この評価方法は、治療をする上で心臓のどこがどのくらい悪いかということがわかりやすく、治療方針を決めるのに有用です。
その反面、AHA分類では心臓全体の壁運動異常がどのくらい悪いのかという量的評価が難しいのが欠点です。
そこで、心臓の壁運動異常を数値化する方法が考えられました。
それがこの記事の主役、LVEF(EF)です。
主役は遅れてやってくるものなのです。
左室造影検査(LVG)によるEF測定
左室造影検査では、心臓を回転楕円体(楕円形を回転させたときにできる形)とみなし、心臓内の血液の量(容積)と、容積の変化を測ることができます。
回転楕円体というと難しく感じますが、ようするにラグビーボールとか地球などの球形に近い形のことです。
心臓が最も大きく拡がった時を左室拡張末期容積、心臓が最も小さく縮んだときを左室収縮末期容積といいます。

拡張末期容積から収縮末期容積を引くと、心臓が1回の収縮あたりに出せる血液量(駆出量: 1回拍出量)がわかります。

心臓の大きさは人によって違います。
心臓の大きい人は駆出量が多く、少ない人は駆出量が少なくなり、駆出量のままだとその数値が良いのか悪いのかがわかりません。
そこで駆出量を拡張末期容積で割って補正し、駆出率に変換します。
上の図を見てもらうとわかりやすいですが、ドーナッツ型の駆出量の面積※を、拡張末期容積の図の面積※で割ると、何パーセントくらい血液を押し出すことができているかが分かるのですね。
※実際は3次元なので面積ではなく容積です。
これが左室駆出率、つまりEFです。
左室駆出率(EF)とは、心臓が収縮したときに自分の大きさに対してどのくらい変化できるか、つまり心臓の壁運動異常をまとめて数値化したもの、ということです。
そして左室駆出率の単位はパーセントですから、EFとは量ではなく単なる割合だということがわかります。
割合に変換することで、心臓の大きさが違っても心臓の動きがよいかどうか、つまり壁運動異常があるかどうかを判断することができるようになります。
EF(左室駆出率)の式は

です。
分数の部分だけだと、出てくる数値は0〜1になり数学的には扱いやすいのですが、一般的にはわかりにくいですね。
そこでわかりやすくパーセント表示にするため100を掛けます。
例えば
- 左室拡張末期容積=100
- 左室収縮末期容積=50
の人を上の式にあてはめると
分数の部分は(100-50) ÷ 100 = 0.5 ですから、パーセント表示するために100倍すると、この人のEFは50%ということになります。
心臓エコー検査によるEF測定が主流
先ほど少し述べたようにEFの測定に左室造影検査しか使えなかったのは昔の話で、今ではEFを測定する他の方法もできました。
左室造影検査の欠点は、
- 血管を切り開いて体内にカテーテルを挿入する
- 造影剤を使いレントゲン撮影をするため放射線被曝が起こり、また腎臓の悪い人には腎臓へ影響が起こることがある
という侵襲性(身体に傷や害を及ぼす傾向があること)です。
そのため、現在ではEFを測定するだけなら侵襲性のない心臓エコー検査(UCG、心エコー)が使われることがほとんどです。

心臓エコー検査(北海道心臓協会フリーイラスト集より)
心臓エコー検査のEF測定方法は2種類あります。
- 左心室内の直径のみを測り左室容積を推定する簡便なTeichholz法(ティーショルズほう)
- 心筋梗塞などの複雑な動きをする心臓で正確なEFを算出するために拡張末期面積と収縮末期面積から容積を求めるSimpson法(シンプソンほう)
です。
左室造影検査で得られるEFと同じ考え方で測定されるのはSimpson法の方です。
昔は画像精度も悪く、計測のための機器の性能も悪かったため、ざっくりとしたTeichholz法しか使えませんでしたが、エコー技術や機器の発達した現在では壁運動異常のある場合は必ずSimpson法を使ったEFを見ておく方がよいでしょう。
ただし、壁運動異常がない場合はTeichholz法による計測のみで問題ないため、Simpson法の測定結果がレポートに記載されていないこともあります。
エコーレポートでは
- (Teich)などと書かれているのがTeichholz法
- (Sim)とか修正Simpson法なら(MOD)などと書かれているEFの数値※がSimpson法
の測定値になります。
※施設によって異なります
心臓エコー検査について詳しく勉強したい方はこちらへどうぞ。
心エコーに詳しくなるオススメ書籍12選 - 心臓リハビリテーションのまにまに
心臓MRI検査では高性能なEF測定が可能
最近では心臓MRI検査(CMR)というものが登場しました。
心臓MRI検査は、左室造影検査や心臓エコー検査に比べ、非常に細かく、しかも色々な方向から心臓を見ることができるのが特徴で、3%のEFの変化も判別できるという報告もあります。
Ejection Fraction - an overview | ScienceDirect Topics
心臓MRIの欠点は機器が高額であること、狭い場所で長時間寝ながら大きな測定音に耐えなければならないこと、金属が身体に埋め込まれている場合は使えないことなどです。
それでも心臓の詳細な評価には非常に有用であり、今後使われる頻度は増えるものと思われます。
EFからわかること
さて、ここまでは歴史的経緯も含めてEFがどういうもので、どうやって測定するのかを説明してきました。
ここまでの話で特に大事なのは
- EFが壁運動異常を客観的に数値化したものである
- EFは量ではなく割合である
ということです。
ここからはEFの数値から何がわかるかを説明していきます。
EFの基準値および収縮能低下の判断方法
EFからわかる最も大事なことは壁運動異常の重症度です。
EFが低いほど壁運動異常が重症であるということです。
EFの正常値は55%〜75%とするのが一般的で、50%以下が軽度低下、40%以下が中等度低下、30%以下が重度低下と考えられています。
(アメリカ心臓病学会によるAHA基準やアメリカ心臓血管呼吸リハビリ協会によるAACVPR基準など、何種類かの基準があるので、必ずしもこの通りではないですが、大体こんな感じです。)
ヨーロッパにおける心不全のガイドラインでは
心不全をEFでグループ分けし、
40%未満をEF低下(HFrEF)
40%〜49%をグレーゾーン(HFmrEF)
50%以上をEFが維持されている(HFpEF)
と分類しています。
こう分けると、
ん?50〜55%はどうなるの?
と感じると思います。
ちなみにEFの正常値は50%台後半でも軽度に低下している、とみなすべきであると報告している研究者もいます。
現在コンセンサスはありませんがEFは
- 55%〜60%あれば壁運動異常はなく正常
- 50%〜55%なら何らかの壁運動異常はあるがほぼ正常で、それだけでは心臓の機能は低下しない
- 50%未満なら低いほど心臓の機能は低下していく
くらいに考えていただけると、壁運動異常の評価として大きく外すことはないかと思われます。
EFが50〜60%で、エコーレポートで壁運動異常あり記載とあるなら、現在何らかの壁運動異常を起こすような軽微な心疾患が存在するか、過去に何かがあった可能性を考えます。
EFが50%未満なら以下に挙げる壁運動異常を起こす疾患の存在を考えます。
EFが低下する原因
EFが低下する病気、つまり壁運動異常が起こる主な病気には、
- 冠動脈が詰まったり狭窄し、心筋が壊死して動かなくなる心筋梗塞をはじめとしたや虚血性心疾患
- 心筋が何らかの理由で変性し、その後心臓が変形して動きが衰える拡張型心筋症などの心筋症
があります。
いずれも心臓の筋肉がなんらかの原因でダメージを受け、動きが悪くなる病気です。
心臓とは筋肉を収縮させて血液を全身に送り出す袋状のポンプですから、筋肉の動きが悪くなる=心臓のポンプが弱くなるということです。
つまり、EFが低下しているならば、壁運動異常により心臓のポンプが弱くなっていると考えて良いでしょう。
EFが40%未満まで大きく低下すると、日常生活くらいの負荷、場合によっては安静時でさえ心臓が送る血液が不足して、心臓以外の部分に影響がでてくる心不全という病気になることもあります。
心不全ってどんな病気? 心不全のリハビリテーションシリーズ その1 - 心臓リハビリテーションのまにまに
このような心不全をHFrEF(へふれふ;heart failure reduced EF, EFの低下した心不全)といいます。
最近まで循環器科や心臓リハビリテーションの主な治療対象はこのEFが低下したHFrEFとその原因になる虚血性心疾患や拡張型心筋症でした。
心不全になると患者さんの予後やADL・QOLが著しく低下するため、どうやってEFの低下する病気を治療するか、どうやってEF低下の進行を予防・治療できるか、ということについては非常に多くの研究が行われてきました。
つい最近まではEFの低下する心筋梗塞や拡張型心筋症、それによる心不全だけが心臓リハビリテーションの対象となっていたのは、そういった理由です。
EF=心機能ではない
最初のほうで心臓で最も大事な指標は心拍出量(CO)だと言いました。
心拍出量は心臓が1分間に何リットルの血液を送り出すことができるか、という数値です。
この血液を送り出すポンプの機能こそが心臓の機能(心機能)と言えます。
ここまで説明してきた通り、EFは壁運動異常の指標で、心臓の収縮の動き(収縮能)を数値化したものです。
つまりEFとは収縮能であり心機能とは別の言葉なのです。
心リハやエコーの初学者、昔勉強したっきりの人は、心機能=EFと捉えることが多いのですが、それが間違いだということがわかります。
ただ、EFがよいということは壁運動異常が無いか軽い異常のみで、収縮能は良いわけです。
ですからEFがよければたくさん血液を出せる心機能がよい心臓だ!と言っても良さそうな気がします。
これは本当でしょうか?
そこで逆の視点、つまり心臓の機能が悪くてもEFがよい場合があるのかを考えてみましょう。
EFが良くてもポンプ機能が悪い場合
次の図をご覧ください。

図の上は正常な心臓で、図の下は何らかの原因で心臓の筋肉が分厚くなった(心肥大)した心臓を表しています。
心臓の外側の大きさは同じにしてあります。
この図から2つのことがわかります。
- 図の上の正常な心臓に比べ、図の下の肥大して中が狭くなった心臓は、左室拡張末期容積(最大容積)が少ない
- そのため肥大した心臓は、なるべくたくさんの血液を出すために正常な心臓よりかなり頑張って収縮し、収縮末期容積を減らしている
つまり心臓にあまり血液をためられないので、壁運動をよくして血液を出しているということです。
これは壁運動異常の逆で、壁運動が過度によいと言え、EFが60%以上と正常な数値になります。
むしろ図の上の心臓より、図の下の心臓のほうがEFが良くなり、EFが70%、時には80%近くになる場合もあります。
それにも関わらず、出せている血液量(心拍出量)で見れば、下の心臓のほうが少なそうですよね。
先ほど、心機能=心拍出量という話をしたのを思い出して下さい。
心機能を心拍出量と考えれば、図の下の肥大した心臓はEFの数値が良くても心拍出量は少ないため、心機能が悪いということができます。
EFが良くても心機能が悪い例がある、ということがお分かりいただけたでしょうか?
ともかく、大事なことは心機能はEFの数値1つでは説明しきれないのだ、ということです。
EFがよい心不全
このようにEFが正常値の55%以上、場合によっては60〜70%以上あっても、心機能が悪い場合があります。
しかし以前はEFがよければ心機能がよいと考えられていたので、EFがよいのに心不全になる患者さんは、場合によってはこれは心不全ではない!みたいに判断されることさえありました。
しかし、近年になって疫学調査などでEFがよくても心不全が発生する例が多数いることが報告されるようになり、臨床現場での認識に変化が起きてきました。
しかもそのようなEFのよい心不全患者さんも、EFの悪い心不全患者さんと同様に寿命が短いことが世界中で次々と報告されたのです。
これがHFpEF(Heart Failure preserved EF: EFの保持された心不全)です。
HFpEFにはいくつかの原因がありますが、その理由の一つが、上でも解説したように中が狭い左心室のEF60%と、正常な左心室のEF60%では数値は同じでも出している血液量が違う、ということです。
ここを押さえておくと、EFがいいのに心不全になるHFpEFという心不全が、心拍出量の観点から理解できるようになるので、頭の片隅に置いておいてください。
そして、このHFpEFには神経体液性因子とリモデリングが大きく関与します。
神経体液性因子についてはこちらで解説しています。
心不全ってどんな病気? 心不全のリハビリテーションシリーズ その1 - 心臓リハビリテーションのまにまに
リモデリングとは、何らかの原因で心拍出量が低下した時に、心臓の形を変えるなどしてそれを補う(代償といいます)変化のことをいいます。
心臓を分厚く肥大させたり、逆に薄く菲薄化させたりするのです。
このようにして、一時的にEFを上げたり、心拍出量を増やしたりしますが、その無理が祟って心機能が低下してくる悪循環に突入するのが、慢性心不全という病気です。
そして悪循環によって心臓は加速度的に悪くなっていきます。
EFがよくても心機能が悪くなる病気とその考え方
EFがよくても心拍出量が少なくなる病気には様々なものがあり、ここでは紹介しきれませんが、代表的なものを挙げておきます。
- 高血圧(性心疾患)
- 心臓弁膜症
- 頻脈性不整脈
- 徐脈性不整脈
- 肥大型心筋症
これらはEFを直接低下させませんが、長期に渡り以下のような原因で心臓に負荷がかかり続けることで、心臓に何らかの変化が起こり、心拍出量が低下してくるというものです。
これらの病気でも重症化してくると、心臓の変形・変性が進んだ結果、壁運動異常が生じてきてEFが低下し始めることもあります。
心機能に関わる5つの因子
ここまでの話で、
EFは心筋の動きの元気さ(心臓の収縮能力)を見る指標で、あくまで心臓の機能に関係する数ある指標のうちの1つにすぎず、心機能をこれ一つだけで表せる指標ではない
ということがお分かりいただけたかと思います。
では心機能には他にどのような因子が関係しているのでしょうか?
心臓のポンプ機能は以下の5つの因子により規定されています。
- 収縮能
- 拡張能
- 前負荷
- 後負荷
- 心拍数
心臓の機能を表す心拍出量は1回拍出量 × 心拍数で計算されます。
1回拍出量(SV: Stroke Volume)とは、1回あたりの左心室の収縮で送れる血液量のことで、実質的な心機能(ポンプ機能)を表すといってもよい非常に大切な指標です。
心拍数以外の4つの因子は、主に1回拍出量に関わります。
4つの因子については
心臓の働きを決める4つの因子 - 心臓リハビリテーションのまにまに
で、そのうちの拡張能については
左室拡張能(E/e')のわかりやすい(かもしれない)解説 - 心臓リハビリテーションのまにまに
で詳しく説明しています。
心拍数以外の4因子のうち、収縮能を代表する指標がここまで説明してきたLVEF(Left Ventricular Ejection Fraction: 左室駆出分画または左室駆出率)です。
EFが悪くない心不全とは、拡張能、前負荷、後負荷、心拍数のどれか、または複数が悪い時に起こります。
また軽度のEF低下と、それ以外の因子が複合して起こる場合もあります。
例えば高齢者の非常に軽い心筋梗塞で、EFはほとんど正常なのになぜかBNP(脳性ナトリウムペプチド)が高いとか肺うっ血などの心不全所見が見られる場合がこのケースに当たります。
もともと他の因子が悪くて心不全になりかけていたところに軽い心筋梗塞による最後の一押しが起こるというパターンですね。
EFを見る時に考えること
ここからは、臨床においてどうやってEFを解釈すればよいのかという話に移ります。
基礎疾患を把握しよう
EFが良くても悪くても、まずは患者さんの心臓病が何かを知らなければ始まりません。
心筋梗塞(虚血性心疾患)の場合
心筋梗塞をはじめとした虚血性心疾患の特徴は、心臓の血管(冠動脈)が詰まったり(閉塞)狭くなったり(狭窄)して、その先にある心筋に酸素が届かなくなって筋肉細胞が死んでしまう(壊死)もしくは酸素不足(虚血)で機能低下することです。
そのため問題が起こった冠動脈の先にある心筋だけ動きが悪くなります。
つまり壁運動異常が一部のみだということです。
これはEFを見るだけではわかりませんので、心エコーなどで壁運動異常の詳細を確認する必要があります。
大体は壁運動という項目やレポートのコメント欄に、どの部位がどのくらい収縮低下しているかが記載されています。
心エコー(UCG)では部位が
- 前壁 (ant; anterior)
- 前壁中隔 (ant-sep, A-S; anterior septal)
- 側壁 (lat; lateral)
- 下壁 (inf; inferior)
- 後壁 (post; posterior)
- びまん性 (diffuse)
に分かれます。
びまん性とは全体にわたって、という意味でこの場合のみ一部ではなく全体を指します。
また壁運動異常の重症度は
- 正常 (normal)
- 軽度低下 (mild hypokinesis)
- 低下 (hypokinesis)
- 重度低下 (severe hypokinesis)
- 無収縮 (akinesis)
- 収縮期膨隆 (dyskinesis)
- 瘢痕化 (scar)
- 心室瘤 (aneurysm)
などがあります。
心筋梗塞などの虚血性心疾患では上の1部位もしくは複数部位に壁運動異常が現れます。
局在性の壁運動異常所見があれば虚血性心疾患がベースにあると疑ってもよいでしょう。
逆に全周性、びまん性の壁運動異常の原因は、心筋梗塞などの虚血性心疾患ではないことが多いです。
このように壁運動異常の場所を確認した上で、EFを見ればどのくらい心臓の収縮能力が落ちているか、つまり心筋梗塞による心臓へのダメージの程度が推測できます。
(心筋梗塞急性期では心筋ダメージ評価はEFよりも心筋トロポニンの上昇やクレアチンキナーゼ: CKの上昇などを用います。心筋梗塞についての別記事で述べる予定です。)
昔、心筋梗塞をした人、いわゆる陳旧性心筋梗塞でも壁運動異常の場所とEFを見ればどのくらいのダメージがあったのか、またその後リモデリングが起きているのかを推測することができます。
この時には、上で紹介したEFの数値とAHA分類などを参考にして壁運動異常の重症度を把握します。
拡張型心筋症(DCM)
拡張型心筋症(DCM)は心臓の筋肉が変性し、心臓が薄くのびてどんどん拡大していく病気です。
拡張型心筋症には、遺伝的なものを始めとし、様々な原因があります。
代表的なものは
- 特発性(遺伝的なもの、原因不明のもの)
- 虚血性(虚血性心疾患がベースのもの)
- 高血圧性(高血圧がベースのもの)
などでしょう。
このうち虚血性のものは上で説明したように壁運動異常が部位ごとにバラバラになります。
一部は重度、残りは軽度などです。
このようなモザイク型の壁運動異常があれば、虚血性心疾患が絡んだEF低下を第一に考えます。
それ以外の全周性に壁運動異常がある場合は、特発性や高血圧性のものが疑われます。
拡張型心筋症は、いずれのパターンでもかなりEFが悪くなるのが特徴です。
なぜなら心臓の筋肉が伸びてしまい、ほぼ役割を果たさなくなっている状態だからです。
この場合もやはり上で紹介したEFの数値から重症度を把握しておきましょう。
拡張型心筋症は、時間経過とともに心臓の拡大と菲薄化が進行し、どんどんと心拍出量やEFが低下していくのが特徴です。
EFが低下する病気には運動療法が効果的
この進行に歯止めをかけたり、場合によっては若干の改善を及ぼす方法として薬物療法と運動療法があります。
リハビリテーション領域における介入では運動療法が重要となります。
当然のことながら、薬物療法が十分行われていて、心臓の状態が落ち着いていることが条件です。
この運動療法のリスク評価項目の1つにEFがあります。
EFによる運動リスク評価
上の方で
- EF30%未満 → 重度低下
- EF40%未満 → 中等度低下
- EF50%未満 → 軽度低下
- EF50%以上 → 正常または軽微低下
としました。
運動や身体活動のリスク評価として考える場合、次のように言い換えることができます。
- EF30%未満 → 超高リスク
- EF40%未満 → 高リスク
- EF50%未満 → 中等度リスク
- EF50%以上 → 低リスク
EFが50%を切っていれば、運動や身体活動が過負荷になることで、心機能が低下したり、ポンプ失調(血圧低下や心源性ショックなど)や致死性不整脈が起こるリスクは上がってきます。
特に30%を切る場合は、かなりリスクが高いと考えてよいでしょう。
このようなケースで運動療法を行う場合は、心肺運動負荷試験(CPX)を行い、至適運動強度を求めることが推奨されます。
心疾患では嫌気性代謝閾値(AT)を超えた運動をしてはいけないのか?無酸素運動と有酸素運動の特徴を知ろう - 心臓リハビリテーションのまにまに
体力(運動耐容能)と酸素摂取量(VO2)とCPXの解説 - 心臓リハビリテーションのまにまに
EFがよくてもリスクが低いわけではない
ただし、ここまで説明したように心機能を決めるのはEFだけではありません。
EFがよいからといって他を何も確認せずに運動処方や身体活動の許可を行うと、心臓のポンプ機能が破綻することがあります。
確認しておいた方がよい事項として
- 心不全の既往がないか
- 中等度〜重度の心臓弁膜症がないか
- 高度な徐脈や頻脈などの不整脈がないか
- コントロール不良の高血圧がないか
などが挙げられます。
心不全既往もしくは中等度の心臓弁膜症があれば、運動処方は心臓リハビリテーション指導士などの専門家の指示を仰ぐのがよいでしょう。
それ以外の重度心臓弁膜症や高度な徐脈や頻脈、コントロール不良の高血圧は運動療法の適応になりません。
EFがよくても悪くても運動は止め、まずは問題となっている状態の治療を優先しましょう。
エコーの一回拍出量係数(SVI)が主流になってくるかも
心臓エコー検査機器の性能向上や測定方法の開発により、かなり正確に一回拍出量(SV)を計測してくれるようになってきています。
特に一回拍出量係数(SVI: stroke volume index)は今後、EFに変わる重要な心機能評価指標になると思われるので、簡単にご紹介しておきます。
SVIは一回拍出量を体格で補正した値で、35以上が正常値です。
SVIの計算には、ドップラー法で計測した一回拍出量(stroke volume)と体表面積を用います。
なぜ体格で補正するかといえば、心臓の大きさはその人の元々の体格に比例するからです。
身体の大きい人は大きな心臓、身体の小さな人は小さな心臓なので、一回拍出量も体格によって変わります。
体表面積(BSA)は次のように計算します。
体表面積 = 身長^0.725 × 体重^0.425 × 0.007184
(^◯は◯乗という意味で、^2なら2乗です)
エコーレポートでBSAがなくても、身長と体重がわかれば自分でSVからSVIを求めることができます。
EFがよくても、SVIが悪い場合は一回拍出量(実際に出している血液量)が落ちているわけですから、EFが良くても心機能は悪いと考えます。
またエコーレポートに心拍数(HR)が記載されていれば、SVI(ml)にHRをかけて、リットル換算すると、最も重要な心機能の値である心係数(CI: Cardiac Index)を算出することができます。
CI = (SV × HR) ÷ (身長^0.725 × 体重^0.425 × 0.007184) ÷ 1000
ですから、
CI = SVI × HR ÷ 1000
です。
心係数がForrester分類における末梢循環不全の指標である2.2を下回る場合、かなりの心拍出量低下があると考えて差し支えありません。
ちなみに僧帽弁や大動脈弁の弁膜症があり、逆流している場合、上のSVには逆流分は反映されていません。
したがって、弁の逆流がある場合は、SVの数値よりも有効血液量はさらに少なくなることは覚えておいてください。
こういう指標が出てくると、EFは壁運動異常の指標であり、心機能の指標ではないことがよく分かりますね。
EFがよくてSVIが悪い時に考えること
誤解を恐れずいえば、SVI < 35 は大きな心疾患の既往の有無に関わらず、既に心不全の領域に入っていると考えてもよいでしょう。
なぜなら心拍出量が低下し始めていると考えられるからです。
AHA/ACCの心不全ステージ分類でいえば、おそらくステージB(心不全は発症していないがなんらかの器質的障害がある)以上になります。
心不全ってどんな病気? 心不全のリハビリテーションシリーズ その1 - 心臓リハビリテーションのまにまに
EFが良いのに心不全になっている人(ステージC〜D)、あるいはSVIが落ちてきている人(ステージB)の場合は、収縮能以外で一回拍出量が落ちる原因がないかを考えます。
この場合は主に拡張能に関わる部分を確認します。
- 左室肥大(心室中隔や後壁の12mm以上の肥厚)がないか
- 左室の狭小化(LVDdがかなり小さな値になっている)がないか
- 左房拡大や心房細動がないか
などです。
またE/e'が13〜15を超えてくる場合は、EFが60%と良い数値でも拡張能が悪く心機能が落ちる場合があります。
ちなみにE/e' ≧13の場合、ヨーロッパ心臓病学会のガイドラインでは心不全を疑う所見に当たります。
E/e' の数値はSVにも反映されますので、SVが少ないのにEFがいい時はE/e' に代表される拡張能障害がある可能性が高くなります。
まとめ
ここまで読んでくださった方は、本当にお疲れ様でした。
最後にわかりやすく内容をまとめておきます。
- EFは収縮能(壁運動異常)を数値化したもの
- EFが悪ければ心臓は悪い
- 心機能=EFではない
- EFがよくても心機能が悪いこともある
- EFは運動療法のリスク評価に使えるけど万能ではない
心機能はEFだけで決まるものではないことを理解すると、逆にEFの重要性と臨床的な意味合いが理解できるようになります。
EFが40%を切るくらい収縮能が悪い人は、疑いなく心機能は低下しています。
またEFが60%以上あるからといって心機能が低下していないと断言できるわけではありません。
臨床でEFについてより深く考えることで、心機能に対する理解を深め、有用な評価につなげていきましょう。
心機能を理解したい方向けに、心機能を決める4つの因子についてこちらで説明しています。ぜひこちらも読んでみて下さい。
心臓の働きを決める4つの因子 - 心臓リハビリテーションのまにまに
おすすめ書籍
心臓エコーについてをより深く知るための本については、こちらで紹介しています。もっと勉強したい人は参考にしてみてください。
リンク先に行くのが面倒な人はこのあたりを読んでいただくのがおすすめです。
心臓外科医が描いた正しい心臓解剖図
心臓エコーの本ではありませんが、基本的な心臓の解剖を美しい絵で非常にわかりやすく説明してくれている良書です。心臓の構造を理解することで心臓エコーだけでなくレントゲンやCT、MRIでの心臓の画像が理解できるようになるはずです。心臓に関わる職種の方はぜひ手元に持っておくとよい一冊。
恋する心エコー ―心機能は4つの線で理解できる―
表紙はちょっと萌え系ですが内容はなかなか硬派で非常に使える一冊と思います。心臓エコーと心機能を両面から理解したい方にはうってつけ。メルクマール編が理解を深めるための説明パート、実践編がその名の通り実践に応用するための内容となっています。
萌える! 心力学 心機能がやさしくわかる58のエピソード
こちらはエコーというよりは心機能とはなにか、ということを理解しやすく説明してくれている一冊です。心臓とはいったいどういう機能をもった臓器なのかを理解するのに最適。
ではでは。



